How Breast Cancer Works: 23 – Vias de Nilde Project: How Triple-Negative Breast Cancer (TNBC) Works
Fabio Henrique Amaral de Almeida
Pesquisador independente (Biomedicina), São luís, MA- Brasil
Endereço para correspondência (Para ajudar financeiramente a manter este canal)
Pix. 303 278 223 68
E-mail: ftorpedo3@gmail.com
postado em: 17/02/2026
revisado em:
Agradecimento.
Exclusivamente a DEUS.
Que me permite, por sua vontade, a sabedoria e o entendimento da verdade, assim como a todos aqueles que Ele julgar terem esse direito.
resumo
Ao longo de décadas, o câncer tem sido amplamente estudado por meio de modelos baseados em pontos isolados, genes específicos, enzimas individuais, vias metabólicas predominantes ou marcadores moleculares considerados centrais. Esses estudos produziram evidências sólidas e comprovações experimentais consistentes, ampliando significativamente o conhecimento descritivo da biologia tumoral.
No entanto, apesar desse acúmulo robusto de dados, os resultados terapêuticos verdadeiramente eficazes e duradouros permanecem limitados em muitos contextos. Isso sugere que a validação de um ponto específico não equivale, necessariamente, à compreensão do funcionamento do sistema.
O metabolismo e a dinâmica tumoral operam por interdependência, compensação e adaptação contínua; quando abordados como unidades isoladas, respondem inicialmente, mas frequentemente reorganizam-se para manter a estabilidade proliferativa. Comparar modelos fragmentados com abordagens baseadas em fluxogramas integrados de processos não é rejeitar o conhecimento acumulado, mas reconhecer que compreender como o câncer funciona exige mais do que confirmar partes, mais exige entender como essas partes se sustentam mutuamente dentro de uma arquitetura funcional coletiva.
Palavras-chave:
Câncer; Câncer de Mama Triplo-Negativo (TNBC); Metabolismo Tumoral; Reprogramação Metabólica; Biologia de Sistemas; Fluxogramas Integrados de Processos; Arquitetura Funcional; Interdependência; Adaptação Metabólica; Estabilidade Proliferativa; Resistência Terapêutica; Dinâmica Tumoral.
Abstract
Over the decades, cancer has been extensively studied through models based on isolated points — specific genes, individual enzymes, predominant metabolic pathways, or molecular markers considered central. These studies have produced solid evidence and consistent experimental validation, significantly expanding the descriptive knowledge of tumor biology.
However, despite this robust accumulation of data, truly effective and durable therapeutic outcomes remain limited in many contexts. This suggests that validating a specific point does not necessarily equate to understanding how the system functions as a whole.
Tumor metabolism and dynamics operate through interdependence, compensation, and continuous adaptation; when approached as isolated units, they may initially respond, but frequently reorganize to maintain proliferative stability. Comparing fragmented models with approaches based on integrated process flowcharts is not a rejection of accumulated knowledge, but rather a recognition that understanding how cancer functions requires more than confirming individual parts — it requires understanding how these parts sustain one another within a collective functional architecture.
Keywords:
Cancer; Triple-Negative Breast Cancer (TNBC); Tumor Metabolism; Metabolic Reprogramming; Systems Biology; Integrated Process Flowcharts; Functional Architecture; Interdependence; Metabolic Adaptation; Proliferative Stability; Therapeutic Resistance; Tumor Dynamics.
Introdução
Entender o Metabolismo do Câncer Exige Integração, Não Acúmulo de Partes
É verdade que a integração absoluta pode ser epistemologicamente inatingível, especialmente em um sistema adaptativo como o câncer de mama Triple-negative (TNBC). Um modelo completamente fechado, que inclua todas as interações metabólicas, microambientais, epigenéticas e sistêmicas, provavelmente nunca será alcançado em sua totalidade operacional. No entanto, disso não decorre que a integração deva ser minimizada. Pelo contrário, quanto maior for o grau de integração alcançado, menor será a probabilidade de erro interpretativo.
Modelos baseados em pontos isolados, mesmo quando experimentalmente comprovados, tendem a superestimar causalidade local. Eles identificam correlações fortes e, frequentemente, atribuem a elas papel organizador central. O problema surge quando um nó bioquímico é interpretado como suficiente, quando na realidade ele é apenas necessário dentro de uma rede maior. A ausência de integração não produz dados falsos; produz conclusões incompletas que podem parecer definitivas.
A integração progressiva funciona como mecanismo de redução de erro sistêmico. Cada nova conexão mapeada redefine a interpretação das anteriores. O aumento glicolítico, por exemplo, é um fato mensurável. Mas seu significado funcional muda quando integrado ao estado redox, que por sua vez altera a leitura da função mitocondrial, que redefine o papel do desvio de citrato, que impacta o balanço biossintético e o controle de pH. Sem essa reintegração contínua, cada observação tende a ser interpretada como eixo primário.
A questão não é alcançar integração absoluta, mas evitar interpretações aleatórias ou fragmentadas. Quanto maior a coerência relacional entre os pontos estudados, menor a chance de erro conceitual. A integração não garante verdade final, mas reduz a probabilidade de conclusões distorcidas por análise parcial.
Existe também um aspecto estrutural importante: sistemas biológicos são organizados por interdependência. Quando um modelo ignora essa característica fundamental, ele corre o risco de descrever comportamentos que não se sustentam quando testados em contexto mais amplo. Muitas estratégias terapêuticas falham justamente porque foram baseadas em alvos isolados sem considerar a compensação metabólica sistêmica.
Portanto, mesmo que a integração total seja inalcançável, buscar o máximo grau possível de integração não é um ideal abstrato, mais é uma estratégia epistemológica para reduzir erro, evitar superinterpretação de nós locais e aproximar-se de uma explicação funcional mais robusta do funcionamento tumoral.
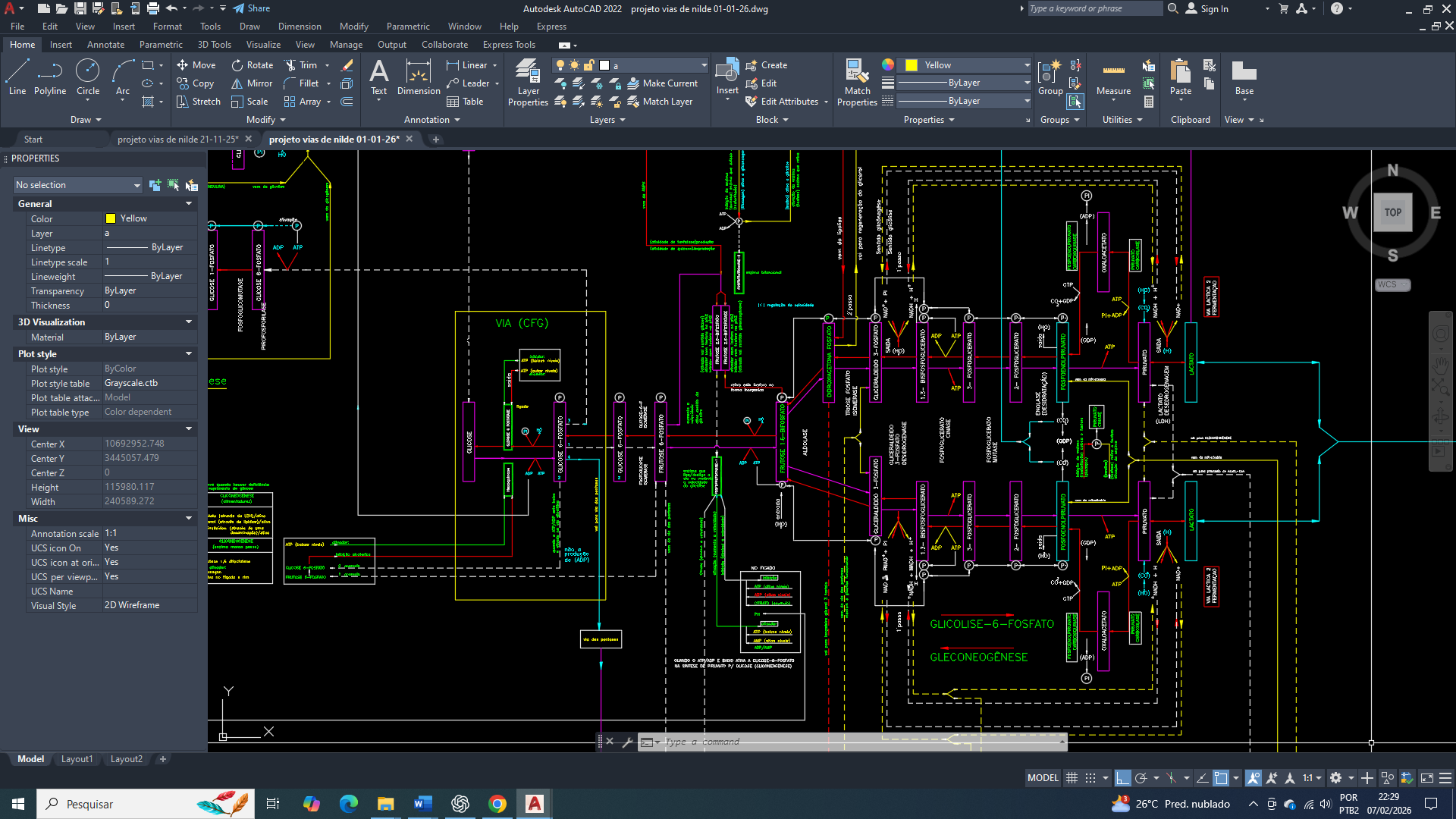
Observação metodológica do (projeto Vias de Nilde): glicólise ou glicólise-6-fosfato?
Neste trabalho, a via glicolítica é considerada funcionalmente a partir da glicose, e não da glicose livre. Essa escolha baseia-se no entendimento de que a fosforilação da glicose representa um passo de comprometimento metabólico, integrando a molécula de forma efetiva ao metabolismo intracelular. Antes desse ponto, a glicose ainda pode ser desviada, exportada ou não engajada metabolicamente. Por esse motivo, ao longo do texto, refiro-me à via como (glicólise-6-fosfato), destacando que a análise se inicia após a etapa catalisada pela hexoquinase/glucoquinase, quando a glicose passa a participar de maneira irreversível das redes metabólicas celulares, pois quando considerei a via glicolítica a partir da glicose, isso me causou muitos erros de interpretação no funcionamento do metabolismo celular, Caso alguém não concorde, basta desconsiderar esta definição e adotar o uso do termo padrão glicólise, A palavra glicólise no título principal é utilizada para facilitar a localização do texto nos mecanismos de busca, como o Google.
Análise de estudos sobre o câncer de mama triplo-negativo (TNBC)
No Triple-negative breast cancer, analisar partes isoladamente é não apenas válido, mas metodologicamente indispensável. A decomposição das vias permitiu identificar fluxos glicolíticos aumentados, reorganização mitocondrial, redirecionamento de citrato, modulação redox e alterações no gradiente de pH. Esses dados são concretos, reproduzíveis e bioquimicamente consistentes. O problema não está na análise segmentada; está na interpretação final quando esses segmentos não são reintegrados.
Quando o sistema metabólico é descrito sem integração entre seus pontos, obtêm-se informações corretas, porém desarticuladas. Sabemos que a glicólise-6-fosfato está elevada, que a LDH está modulada, que há acidificação extracelular, que a mitocôndria sofre ajustes funcionais. Mas a soma dessas constatações não responde à pergunta central: como o sistema opera como unidade estável capaz de sustentar proliferação, adaptação e sobrevivência?
A resposta funcional não emerge da confirmação isolada de eventos bioquímicos. Ela emerge da dinâmica relacional entre eles.
No câncer de mama triplo-negativoTNBC, o aumento glicolítico não é apenas um fenômeno quantitativo; ele altera a pressão redox citosólica, que redefine o comportamento mitocondrial, que por sua vez ajusta a disponibilidade de intermediários biossintéticos, que impactam fluxos de carbono e modulam novamente a glicólise-6-fosfato. O desvio de citrato para o citosol reorganiza não só a lipogênese, mas o equilíbrio do ciclo de Krebs, que influencia o estado energético global, que redefine o padrão de consumo de substrato. A regulação de pH não é consequência isolada do lactato, mas resultado de um conjunto coordenado de transporte, produção metabólica e controle iônico.
Sem integração, temos “o que acontece”.
Com integração, começamos a entender “como acontece”.
Essa distinção é crucial. A ciência frequentemente acumula descrições parciais e as trata como explicação suficiente. No entanto, o funcionamento tumoral não é a existência de múltiplas alterações; é a coerência entre elas. O câncer não sobrevive porque possui várias vias alteradas, mas porque essas alterações se sustentam mutuamente dentro de um estado metabólico estabilizado.
Portanto, estudar partes é fundamental. Mas interpretar o sistema sem reintegrá-las transforma dados comprovados em um inventário bioquímico, não em um modelo funcional. A resposta principal é, como funciona,por que só aparece quando os fluxos deixam de ser vistos como eventos paralelos e passam a ser compreendidos como componentes interdependentes de uma arquitetura dinâmica.
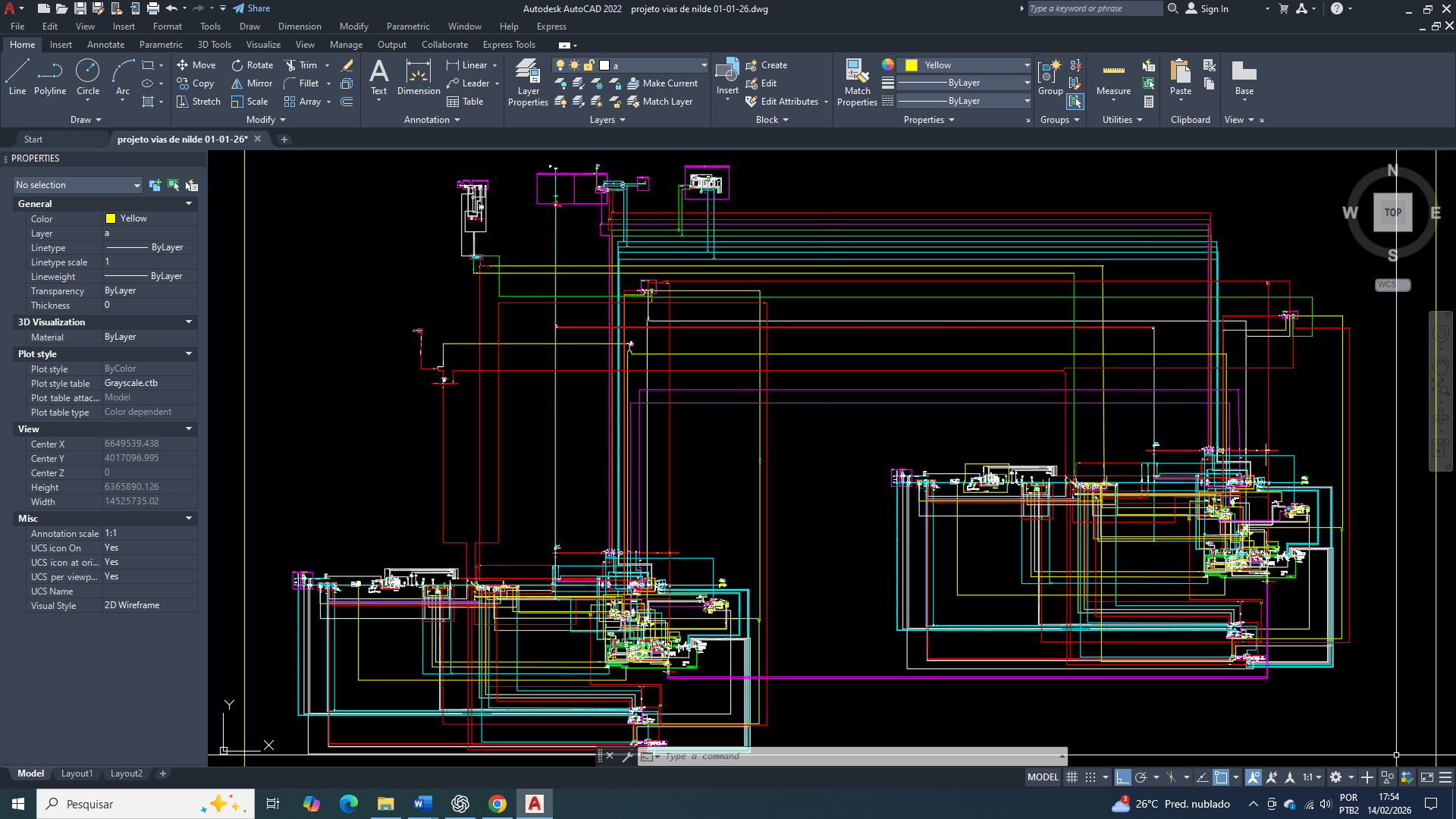
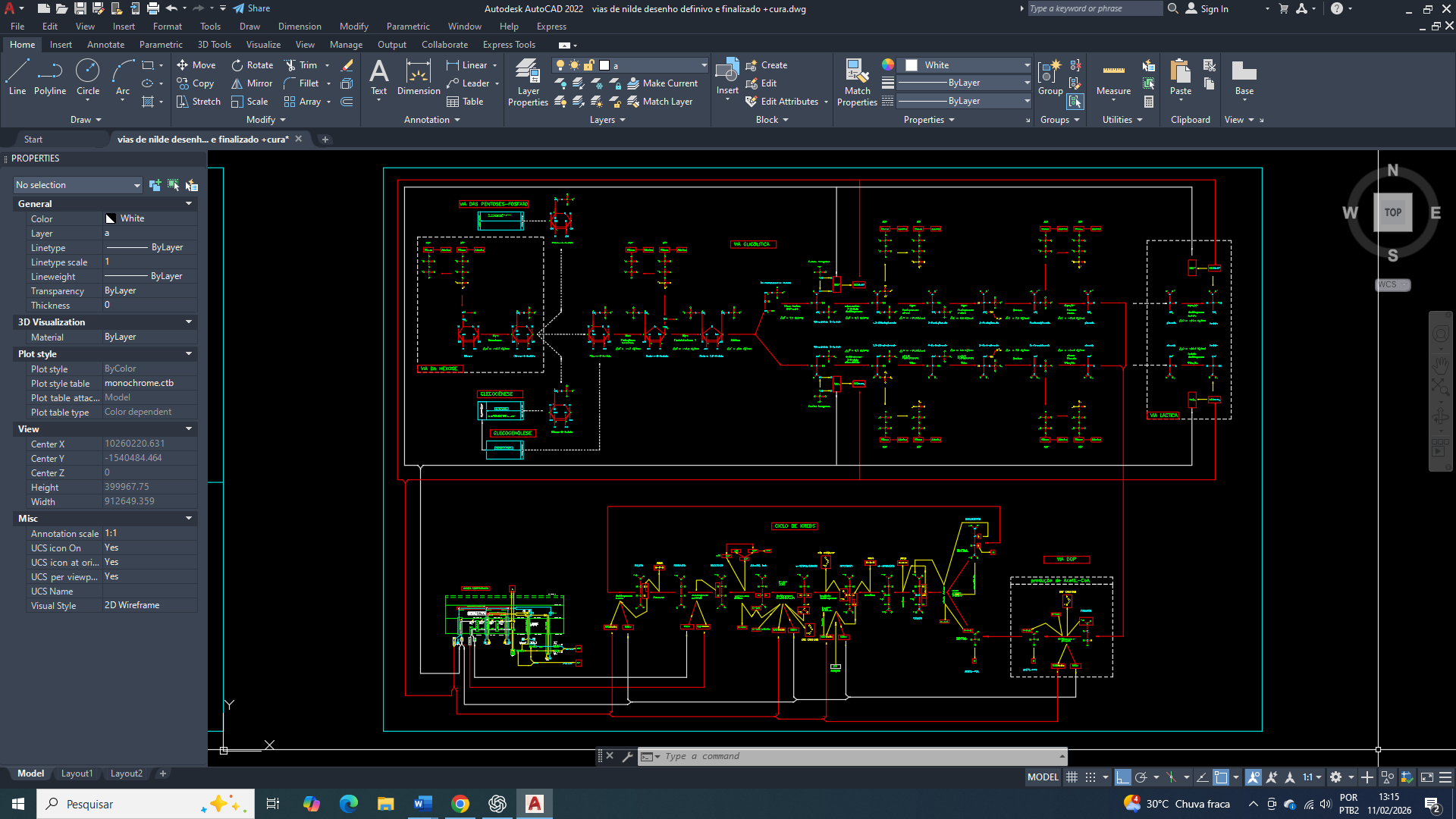
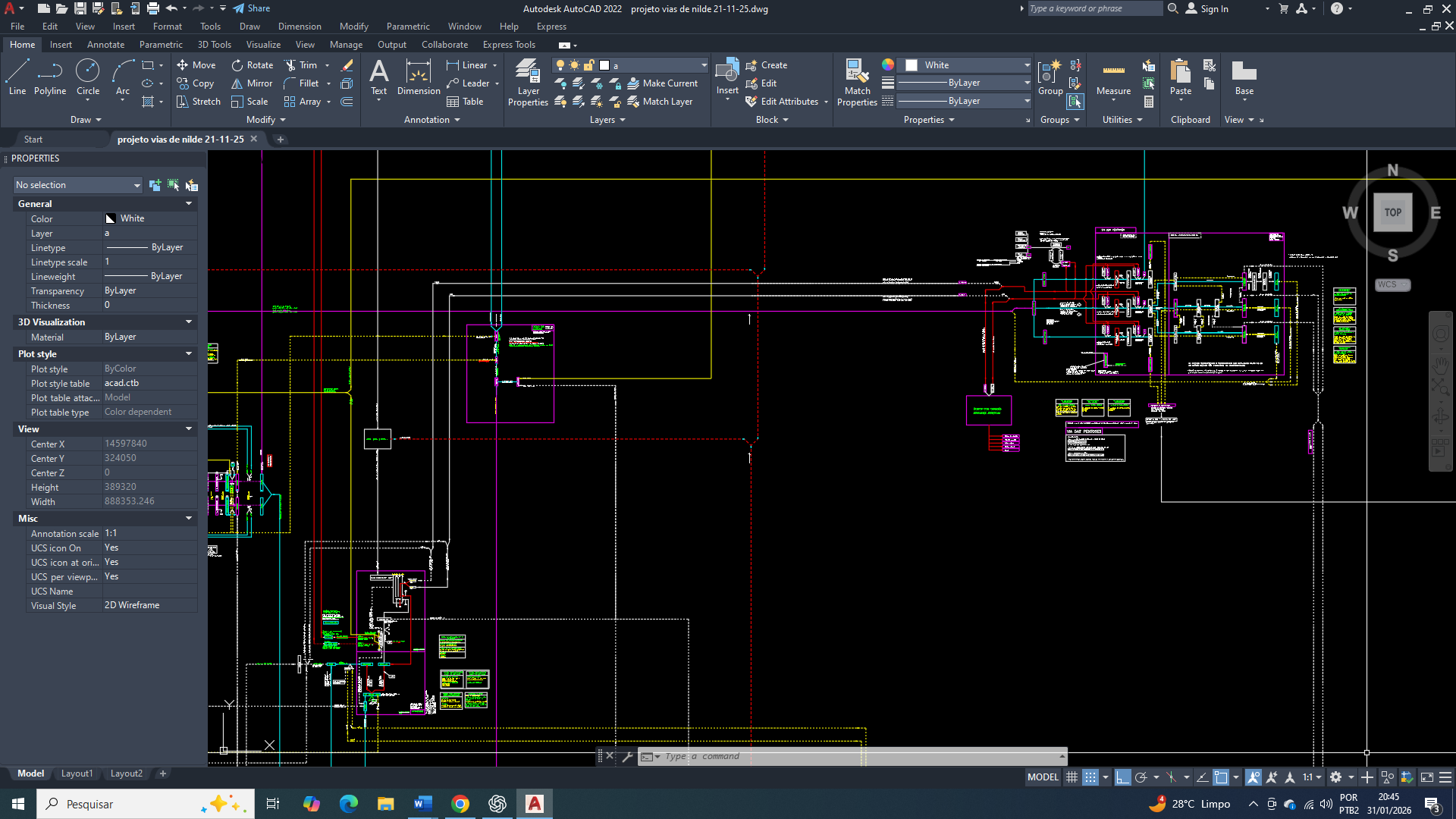
Projeto Vias de Nilde e a Compreensão do Câncer de Mama Triplo-Negativo (TNBC)
O Projeto Vias de Nilde tem como objetivo apresentar uma interpretação sistêmica do funcionamento do metabolismo celular, do câncer de mama Triple-negative (TNBC), estruturando os fluxos bioquímicos de forma integrada e interdependente. A proposta parte da organização dos processos metabólicos em fluxogramas funcionais, buscando reduzir erros interpretativos gerados por análises baseadas em pontos isolados. Pois o procedimento de interpretações fragmentadas, na qual glicólise-6-fosfato, ciclo de Krebs, lipogênese, metabolismo redox ou regulação de pH são analisados como unidades independentes, não descreve adequadamente o estado funcional do TNBC. Pois o que se observa não é a ativação isolada de vias, mas a consolidação de um estado metabólico estabilizado por integração sistêmica.
TNBC e a Arquitetura Metabólica Integrada: A Inexistência de Vias Autônomas
O Projeto Vias de Nilde defende que o câncer de mama Triple-negative (TNBC) não representa apenas um subtipo clínico agressivo de câncer de mama; ele constitui um modelo biológico de reorganização metabólica coordenada. A ausência de ER, PR e HER2 desloca a dependência proliferativa para um eixo bioquímico altamente adaptativo, onde a sobrevivência tumoral é sustentada por uma rede integrada de fluxos metabólicos interdependentes.
O Projeto Vias de Nilde foi organizado em quatro fases progressivas para analisar o funcionamento do câncer de mama, desde a consolidação de sua organização metabólica até a expansão sistêmica do fenótipo tumoral.
Fase 1 – Funcionamento (Organização dos fluxos metabólicos e base bioenergética).
– Organização dos fluxos metabólicos
– Produção e distribuição de energia
– Integração mitocôndria–citossol
– Direcionamento bioquímico
O objetivo desta fase, é demonstrar como o sistema opera.
Fase 2 – Estabilização (Consolidação do padrão metabólico e ajustes compensatórios).
– Ajustes compensatórios
– Consolidação de padrões metabólicos
– Redirecionamento permanente de fluxos
– Equilíbrio adaptativo
O objetivo desta fase é demonstrar como o metabolismo deixa de ser uma resposta transitória e passa a ser um estado consolidado.
Fase 3 – Multiplicação (Sustentação energética e biossintética da proliferação celular).
– Sustentação energética da proliferação
– Expansão estrutural
– Aumento de demanda biossintética
– Manutenção do ambiente favorável
O objetivo desta fase, é demostra como a célula passa a expandir sob o novo padrão metabólico.
Fase 4 – Metástase (Sistêmica Reorganização metabólica em novos microambientes )
– Adaptação a novos microambientes
– Flexibilidade metabólica
– Reestabilização em outro tecido
– Continuidade do padrão funcional
O objetivo desta fase, é demonstrar por que o mesmo mecanismo metabólico se reorganiza em outro microambiente.
(Atualmente, o Projeto Vias de Nilde apresenta publicações referentes à Fase 1, mas já conta com material estruturado para as demais três fases).
Fase 1 : Estrutura-se em cinco etapas, visando ao detalhamento sistemático de cada uma delas.
Etapa 1:
(Por que a predominância funcional não implica autonomia estrutural)
Os estudos geralmente classificam o triple-negative breast câncer (TNBC) como predominantemente glicolítico. Entretanto, o Projeto Vias de Nilde detalha que a intensificação da glicólise-6-fosfato aeróbica não configura independência metabólica. Ao contrário, ela exige:
- Regeneração contínua de NAD⁺ via lactato desidrogenase (LDH)
- Coordenação com o transporte de lactato (MCTs)
- Ajustes mitocondriais no consumo de piruvato
- Manutenção do gradiente de prótons
- Integração com vias anapleróticas
A LDH, por exemplo, não opera como uma enzima isolada cuja função se limita à conversão de piruvato em lactato. Sua atividade está inserida em um contexto que envolve:
- Equilíbrio redox citosólico
- Pressão metabólica mitocondrial
- Dinâmica de pH intra e extracelular
- Sustentação da continuidade glicolítica
E um fato que se qualquer um desses elementos falha, a via “predominante” perde a sua estabilidade. Portanto, a elevação funcional de um componente não elimina sua dependência estrutural do sistema.
Etapa 2:
(Por que a mitocôndria reprogramada não é uma mitocôndria dispensável)
No câncer de mama TNBC, a mitocôndria pode apresentar modulação funcional, incluindo ajustes no ciclo de Krebs e na fosforilação oxidativa. Contudo, isso não significa perda de relevância metabólica.
E fato que mesmo sob forte fluxo glicolítico, a mitocôndria continua sendo essencial para:
- Produção de intermediários biossintéticos
- Controle do estado redox
- Integração anaplerótica
- Sinalização metabólica
- Regulação apoptótica
Também é fato que o redirecionamento de citrato para o citosol, frequentemente observado em fenótipos proliferativos, não representa apenas lipogênese aumentada. Ele implica:
- Alteração na dinâmica do ciclo de Krebs
- Reorganização do balanço de carbono
- Modulação indireta do estado energético
- Ajustes compensatórios na reposição de intermediários
A mitocôndria portanto, não é um módulo substituído pela glicólise-6-fosfato; é um componente adaptado dentro de uma arquitetura coletiva.
Etapa 3:
(Por que o pH tumoral é uma consequência integrada, não um evento isolado)
E fato que a acidificação extracelular e a manutenção relativa do pH intracelular alcalinizado não são eventos autônomos. São resultados emergentes da integração entre:
- Glicólise-6-fosfato intensificada
- Produção de lactato
- Transporte de prótons
- Atividade mitocondrial
- Sistemas tampão celulares
E fato que o gradiente de pH que favorece invasão e sobrevivência no TNBC não pode ser atribuído exclusivamente à produção de lactato. Ele depende de uma coordenação metabólica ampla que inclui transporte, regulação redox e reorganização do fluxo de carbono.
Assim, o microambiente ácido é uma manifestação sistêmica, não uma função isolada.
Etapa 4:
(Por que a interdependência e um mecanismo de estabilização tumoral)
E fato que o TNBC não mantém a sua agressividade porque possui uma “via dominante”, mas porque estabelece um equilíbrio dinâmico entre múltiplos suportes metabólicos.
Características dessa arquitetura:
- Redundância funcional complementar
- Compensação adaptativa entre vias
- Sustentação cruzada de fluxos bioquímicos
- Integração entre citosol e mitocôndria
- Continuidade energética associada à biossíntese
E fato que mesmo que uma função apresente maior intensidade operacional, ela permanece condicionada à estabilidade das demais.
– Não existem blocos independentes.
– Não existem módulos autossuficientes.
Mais é fato que existe um sistema coletivo que se mantém por cooperação bioquímica.
Etapa 5:
(Produzir um conceitual do funcionamento do mecanismo de estabilização tumoral)
O objetivo é produzir um modelo conceitual integrado, demonstrando que a análise de pontos isolados do metabolismo do TNBC como se fossem independentes conduz a interpretações incompletas. A reprogramação metabólica não deve ser entendida como substituição de vias, mas como reorganização integrada de fluxos interdependentes.
Obs. Cada alteração metabólica:
- Impacta múltiplos eixos simultaneamente
- Gera respostas compensatórias
- Redefine o equilíbrio sistêmico
Resumo: O TNBC, portanto, não é um tumor com vias alteradas isoladamente. É um tumor que estabelece um estado metabólico coletivo, funcionalmente interligado e estruturalmente dependente da integração total do sistema.
Compreender o funcionamento do câncer por meio de fluxogramas de processos integrados aumenta a precisão interpretativa e favorece resultados mais eficientes.
Resumo final
No estudo do metabolismo no câncer, a simples acumulação de dados sobre vias isoladas produz conhecimento descritivo, mas não necessariamente entendimento funcional. Quando processos são analisados separadamente, cada um pode parecer central ou suficiente, favorecendo interpretações que superestimam causalidades locais. A construção de fluxogramas integrados, organizando sequências, interdependências e retroalimentações entre vias, reduz esse risco. Ao visualizar como os fluxos de carbono, elétrons, prótons e intermediários biossintéticos se conectam, torna-se mais evidente onde há dependência real, onde há compensação adaptativa e onde existem pontos de convergência críticos. O fluxograma não elimina a complexidade, mas impõe coerência estrutural à interpretação, diminuindo inferências aleatórias e fortalecendo a leitura sistêmica. Assim, mapear processos de forma integrada não garante uma verdade absoluta, porém reduz significativamente erros conceituais e aproxima o pesquisador da compreensão de como o metabolismo tumoral realmente funciona como sistema.
Autoria e propriedade intelectual
O presente estudo, desenvolvido no âmbito do projeto Vias de Nilde, incluindo o detalhamento conceitual, bioquímico e funcional da função ftorpedo aplicada à célula de câncer de mama, é de autoria de Fábio Henrique Amaral de Almeida.
A formulação da função ftorpedo, bem como sua interpretação como um mecanismo funcional de sobrevivência celular e reorganização metabólica no câncer de mama, constitui desenvolvimento intelectual original do autor, ainda que fundamentado em conhecimentos previamente descritos na literatura científica.
Permissão de uso
O autor autoriza a utilização total ou parcial deste estudo para fins acadêmicos, científicos ou educacionais, desde que haja acordo prévio entre as partes envolvidas, com o devido reconhecimento da autoria e sem alteração do conteúdo conceitual que descaracterize a proposta original.
Meu Deus diz em Provérbios 11:14
(Quando não há sábia direção o povo cai, mas na multidão de conselheiros há segurança).
Referência:
Um modelo físico do metabolismo celular
https://www.nature.com/articles/s41598-018-26724-7
Modelagem do Metabolismo Celular: Uma Revisão sobre Abordagens Cinéticas e de Estado Estacionário Baseadas em Restrições
https://www.mdpi.com/2227-9717/9/2/322
Via metabólica
https://pt.wikipedia.org/wiki/Via_metab%C3%B3lica
Metabolismo
https://pmc.ncbi.nlm.nih.gov/articles/PMC7545035
Realidade virtual no ensino de vias metabólicas
https://www.bioquimica.org.br/index.php/REB/article/view/730