Fabio Henrique Amaral de Almeida
Pesquisador independente (Biomedicina), São luís, MA- Brasil
Endereço para correspondência (Para ajudar financeiramente a manter este canal)
Pix. 303 278 223 68
E-mail: ftorpedo3@gmail.com
postado em: 28/01/2026
revisado em:
Agradecimento.
Exclusivamente a DEUS.
Que me permite, por sua vontade, a sabedoria e o entendimento da verdade, assim como a todos aqueles que Ele julgar terem esse direito.
Resumo
A acetil-CoA carboxilase (ACC) como eixo metabólico na reprogramação do câncer de mama
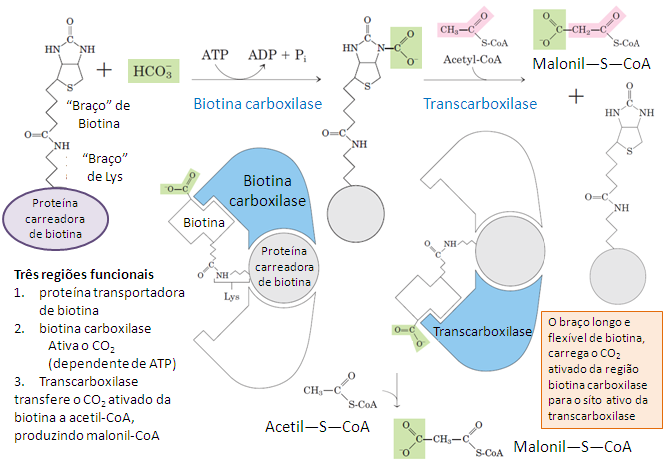
A acetil-CoA carboxilase é uma enzima multicomponente altamente regulada, cujo funcionamento depende da integração precisa entre os domínios biotina carboxilase (BC), carreador de biotina (BCCP) e carboxiltransferase (CT). Essa coordenação permite a ativação do CO₂, o transporte da biotina e a transferência eficiente do grupo carboxila para o acetil-CoA, culminando na formação de malonil-CoA. No câncer de mama, esse processo adquire relevância patológica, pois sustenta a lipogênese aumentada característica das células tumorais.
A atividade da ACC é modulada por múltiplos níveis de controle, incluindo fosforilação dependente de AMPK, sinalização insulínica, disponibilidade de citrato citosólico e integridade estrutural da enzima. A desregulação desses mecanismos favorece a manutenção de um estado lipogênico ativo, contribuindo para a adaptação metabólica tumoral. Assim, a ACC emerge não apenas como uma enzima chave do metabolismo lipídico, mas como um elo crítico entre sinalização celular, organização estrutural enzimática e progressão do câncer de mama, tornando-se um alvo conceitual e terapêutico de grande interesse.
Palavras-chave
Acetil-CoA carboxilase; Câncer de mama; Lipogênese; Reprogramação metabólica; Sinalização por AMPK; Malonil-CoA; Síntese de ácidos graxos
Abstract
Acetyl-CoA carboxylase (ACC) is a highly regulated multicomponent enzyme whose activity depends on the precise integration of the biotin carboxylase (BC), biotin carboxyl carrier protein (BCCP), and carboxyltransferase (CT) domains. This coordination enables CO₂ activation, biotin-mediated group transfer, and efficient carboxyl group transfer to acetyl-CoA, culminating in malonyl-CoA formation. In breast cancer, this process acquires pathological relevance, as it sustains the elevated lipogenesis that characterizes tumor cells.
ACC activity is modulated at multiple regulatory levels, including AMPK-dependent phosphorylation, insulin signaling, cytosolic citrate availability, and structural integrity of the enzyme. Dysregulation of these mechanisms favors the maintenance of an active lipogenic state, supporting metabolic adaptation in tumor cells. Thus, ACC emerges not only as a key enzyme in lipid metabolism but also as a critical link between cellular signaling, enzymatic structural organization, and breast cancer progression, making it a relevant conceptual and therapeutic target.
Keywords
Acetyl-CoA carboxylase; Breast cancer; Lipogenesis; Metabolic reprogramming; AMPK signaling; Malonyl-CoA; Fatty acid synthesis
Introdução
Importância de compreender o funcionamento da acetil-CoA carboxilase (ACC)
A acetil-CoA carboxilase (ACC) ocupa uma posição muito importante no metabolismo celular por ser responsavel em catalisar a etapa limitante da síntese de ácidos graxos, Pela conversão de acetil-CoA em malonil-CoA. Em condições fisiológicas, essa enzima tem a função de atua como um ponto de integração entre o estado energético celular, sinais hormonais e a disponibilidade de nutrientes. No contexto do câncer de mama, entretanto, a ACC não é apenas um componente metabólico basal e passa também a desempenhar um papel estratégico de grande importância na reprogramação metabólica tumoral.
Células de câncer de mama apresentam elevada demanda por lipídios, necessários não apenas para a produção de membranas celulares, mas também para a geração de sinais lipídicos, modulação redox e sustentação da proliferação descontrolada. A ativação persistente da ACC favorece a um acúmulo de malonil-CoA e impulsiona a lipogênese de novo, que é um processo intimamente associado à progressão tumoral, permitindo uma agressividade e resistência terapêutica. Dessa forma, é essencial compreender o funcionamento molecular da ACC, desde a sua organização estrutural até a sua coordenação entre seus domínios catalíticos, também torna-se essencial para interpretar como e porque acontece essas alterações metabólicas que sustentam o fenótipo maligno no câncer de mama.
Estrutura da acetil-CoA carboxilase (ACC)
A acetil-CoA carboxilase (ACC) é uma enzima multifuncional cuja a sua atividade depende da integração estrutural precisa entre três componentes catalíticos, que são a biotina carboxilase (BC), a proteína carreadora de carboxil-biotina (BCCP) e a carboxiltransferase (CT). Esses componentes formam um sistema coordenado no qual através de eventos químicos espacialmente separados são integrados por rearranjos conformacionais e pela mobilidade controlada da biotina ligada covalentemente à enzima. A compreensão detalhada da estrutura de cada um desses domínios é essencial para explicar o funcionamento da ACC como uma holoenzima.
Hierarquia de funcionamento da Estrutura da acetil-CoA carboxilase (ACC):
- Sub-processo 1 → Biotina carboxilase (BC)
- Sub-processo 2 → Domínio carreador de biotina (BCCP)
- Sub-processo 3 → Carboxiltransferase (CT)
Biotina carboxilase (BC)
Sub-processo 1 – dividido em 02 partes
A estrutura da BC seguida da organização dos domínios A e C, com uma dinâmica conformacional do domínio B, permitindo a ligação do ATP, o que possibilita a ativação do bicarbonato, levando à formação do carboxifosfato e também à geração de CO₂ reativo, que vai promover a ativação da biotina, resultando na formação da carboxil-biotina, a qual vai ser transportada pelo BCCP até a CT, é lá onde ocorre o reconhecimento do complexo, a descarboxilação da biotina e também a transferência do grupo carboxila para o acetil-CoA, culminando na formação do malonil-CoA e na regeneração funcional do BCCP, garantindo que aja uma continuidade do ciclo catalítico da ACC.
Parte -1 (Organização estrutural conservada da BC)
A proteína biotina carboxilase (BC) dá nome à família das biotina carboxilases e constitui um tipo de modelo estrutural representativo dessa família de proteínas, conforme é classificado no banco Pfam.
A primeira estrutura resolvida da subunidade BC revelou que essa enzima é uma proteína homodimérica, onde cada monômero é constituído por 449 resíduos de aminoácidos, com uma massa molecular com aproximadamente 49,4 kDa. O domínio biotina carboxilase é responsável pela ativação do bicarbonato e também pela etapa inicial de carboxilação da biotina.
Entrada: cadeia polipeptídica da BC
Por que passa por este processo: a função catalítica depende da correta organização tridimensional
Produto final: monômero estruturalmente funcional, capaz de formar domínios catalíticos
Parte – 2 (Formação do núcleo estrutural do sítio catalítico)
Estruturalmente, a BC se apresenta com uma organização altamente conservada e composta por três domínios bem definidos por monômero, denominados domínios A, B e C. Onde os domínios A e C formam a porção globular principal da proteína.
Entrada: domínios A e C organizados
Por que passa por este processo: esses domínios constituem a base física do sitio ativos
Produto final: núcleo catalítico apto à ligação de substratos
O domínio A
(resíduos 1–103) é constituído por folhas β paralelas flanqueadas por hélices α, formando uma arquitetura típica de proteínas da família das biotina carboxilases. Esse domínio tem a função de contribuir de maneira direta para a formação do sítio ativo e também para participar da ancoragem da molécula de ATP.
Função do domínio A – Reconhecimento e ancoragem do ATP (Formação do domínio A e contribuição para o sítio ativo)
Entrada: ATP e domínio A corretamente estruturado
Por que passa por este processo: o ATP é necessário para ativar o bicarbonato
Produto final: ATP estabilizado no sítio catalítico
O domínio B – (dividido em 02 etapas)
é encontrado em proteínas da família das carbamoilfosfato sintases, correspondendo a uma região estruturalmente flexível da proteína, que se estende para fora da porção globular, dobrando-se em duas cadeias do tipo α-hélice e três cadeias β. Essa formação é essencial para que haja uma dinâmica catalítica, que é caracterizada por catalisar as reações em que a molécula de ATP é utilizada para ativar o bicarbonato.
Esse domínio se caracteriza por ser uma região altamente móvel, que se lança para frente a partir da estrutura globular formada pelos domínios A e C. Durante o ciclo catalítico, o domínio B sofre mudanças conformacionais significativas, alternando entre conformações aberta e fechada.
Função da etapa 1 – Dinâmica conformacional do sítio ativo
Entrada: BC com ATP ligado
Por que passa por este processo: o fechamento do domínio B organiza e isola o sítio catalítico
Produto final: sítio ativo fechado e cataliticamente competente
A etapa 1 tem a função da ligação da molécula de ATP é induzir um rearranjo estrutural que promove o fechamento do domínio B sobre o sítio catalítico, que é caracterizado por uma rotação aproximada de ~45° em direção ao núcleo da proteína. Esse movimento assegura o correto posicionamento dos substratos, estabiliza intermediários reativos e também isola temporariamente o sítio ativo, aumentando a eficiência catalítica.
Função da etapa 2 – Ativação do bicarbonato
Entrada: ATP ligado + bicarbonato
Por que passa por este processo: o bicarbonato precisa ser ativado para gerar CO₂ reativo
Produto final: intermediário carboxifosfato
O domínio C
Tem a função de complementar esse domínio globular e também apresenta uma organização estrutural complexa, que é composta por folhas β antiparalelas intercaladas por hélices α. Esse domínio corresponde a uma região globular da proteína que é formada por uma folha β principal contendo oito cadeias β antiparalelas, além de uma segunda folha β menor, composta por três cadeias β antiparalelas, associadas a sete hélices α.
Essa composição estrutural, em conjunto com o domínio A, constitui a base estrutural do sítio catalítico, no qual resíduos que são provenientes desses dois domínios cooperam para a coordenação do ATP, do bicarbonato e também do íon magnésio, enquanto que o domínio B vai contribuir para o mecanismo de fechamento e para a dinâmica do sítio ativo.
A biotina carboxilase apresenta um sítio catalítico cuja a sua arquitetura depende principalmente da contribuição dos domínios A e C, nos quais se concentram os resíduos envolvidos na ligação e no posicionamento dos substratos. Diferentemente desses domínios, o domínio B não integra o núcleo estrutural do sítio ativo, mas ele exerce um papel que é determinante na dinâmica catalítica da enzima. Porque durante o ciclo de reação, esse domínio sofre um rearranjo estrutural expressivo que vai resultar em um fechamento transitório do sítio catalítico, caracterizando estados estruturais distintos da proteína.
Embora essa organização geral da biotina carboxilase seja conservada entre organismos, a enzima de origem eucariótica, ela apresenta extensões adicionais em sua sequência primária. Essas inserções ocorrem predominantemente na região que conecta os domínios A e B e resultam em uma proteína com tamanho maior (com aproximadamente ~550 resíduos), sem alterar o seu arranjo funcional que é essencial no domínio catalítico.
Função do dominio C – Coordenação catalítica dos cofatores
Entrada: ATP, bicarbonato e Mg²⁺
Por que passa por este processo: a catálise depende da estabilização eletrostática
Produto final: complexo catalítico organizado para reação química
Funcionamento da biotina carboxilase (BC)
Ativação do bicarbonato dependente de ATP
A biotina carboxilase (BC) catalisa a carboxilação da biotina por meio de um mecanismo dependente de ATP, no qual o bicarbonato é inicialmente ativado. Durante essa etapa, o bicarbonato reage com o fosfato γ do ATP, resultando na formação de um ADP e de um intermediário carboxifosfato que é altamente instável. A rápida decomposição desse intermediário leva à liberação de fosfato inorgânico e o dióxido de carbono (CO₂).
Ativação da biotina e formação da carboxil-biotina
O fosfato inorgânico formado tem a função de atua como base, promovendo a desprotonação do átomo N1 da biotina que permiti a formação de um intermediário enolato. Esse estado intermediário é estabilizado por resíduos conservados do sítio catalítico, isto vai possibilitar que o CO₂ que foi gerado ataque o átomo N1 desprotonado. Tendo como o resultado, que vai forma o carboxil-biotina, covalentemente ligada ao domínio transportador de biotina (BCCP).
Transferência do grupo carboxila para a carboxiltransferase
Após a reação de carboxilação, a carboxil-biotina é direcionada para o sítio ativo da carboxiltransferase (CT), onde lá vai ocorrer a descarboxilação da biotina e também a transferência do grupo carboxila para o acetil-CoA, finalizando a formação de malonil-CoA. Esse processo envolve uma coordenação que deve ser precisa entre os movimentos estruturais e eventos catalíticos, assegurando uma eficiência global da reação.
Organização modular do sítio de ligação do ATP
O sítio de ligação do ATP na biotina carboxilase humana apresenta uma organização modular, que é composta por 03 regiões funcionalmente distintas
1 – Região de reconhecimento da base adenina
Essa é a região responsável pelo reconhecimento da base adenina que envolve os resíduos E201, K202, L204, I157–K159, L278 e I287, os quais participam de interações específicas que promovem a estabilização da base nitrogenada do ATP.
2 – Região de interação com a ribose
Essa é a região de interação com a ribose que é composta, entre outros, pelos resíduos H209, Q233, H236 e H438, que tem a função de contribuir para o posicionamento adequado do anel ribose no sítio catalítico.
3 – Região de ligação dos grupos fosfato
Essa é a região que tem a função de ligação aos grupos fosfato que vão envolver resíduos carregados positivamente, além da coordenação do íon Mg²⁺, os quais atuam na neutralização das cargas negativas dos fosfatos e em uma orientação correta do ATP para a catálise.
Essas regiões atuam de forma cooperativa para posicionar corretamente o nucleotídeo no sítio catalítico, garantindo uma ativação eficiente do bicarbonato e a progressão ordenada das etapas da reação catalítica. Sendo que esse arranjo estrutural é fundamental para a atividade catalítica da enzima.
Dimerização e mecanismo catalítico do tipo flip-flop
A biotina carboxilase (BC) é uma proteína dimérica, e os sítios ativos de cada monômero são estruturalmente completos e são cataliticamente ativos. Esses sítios catalíticos localizam-se afastados da interface dimérica e, do ponto de vista estrutural, se apresentam com independência para a formação do motivo catalítico. Mesmo assim, a dimerização é essencial para a que aja uma plena atividade enzimática, uma vez que a catálise ocorre de maneira alternada entre os dois sítios ativos, caracterizando um ciclo catalítico que opera por um mecanismo do tipo flip-flop.
A interface de ligação entre os monômeros é mediada através de interações iônicas específicas, que envolvem os resíduos Arg19 e Glu23 de um monômero com os resíduos Glu408 e Arg401 do monômero adjacente, respectivamente.
Interações específicas no sítio ativo
Os resíduos de aminoácidos que são importantes para a interação com o bicarbonato são R292, V295 e E296, que interagem, respectivamente, com os átomos de oxigênio 1, 2 e 3 da molécula de bicarbonato. Já os resíduos Y82, V295 e R338 participam na interação da biotina com o sítio ativo da BC.
A interface de associação entre os monômeros é estabilizada principalmente por interações iônicas específicas, envolvendo os resíduos Arg19 e Glu23 de um monômero em contato com os resíduos Glu408 e Arg401 do monômero que é adjacente, respectivamente. Essas interações tem a fumção decontribuir para a estabilidade estrutural do dímero e para o correto funcionamento catalítico da enzima.
No sítio ativo, a interação com o bicarbonato envolve resíduos específicos de aminoácidos. O resíduo Arg292, o Val295 e o Glu296 participam da coordenação do bicarbonato através de interações com seus átomos de oxigênio O1, O2 e O3, que vão respectivamente, favorecer a sua ativação para a reação de carboxilação.
A interação da biotina com o sítio catalítico da BC sempre envolve, (entre outros), os resíduos Tyr82, Val295 e Arg338, que contribuem para o correto posicionamento da molécula de biotina durante a formação do intermediário carboxilado. Além disso, o íon magnésio, é essencial para a estabilização dos nucleotídeos fosfatados, interage com os resíduos Glu276 e Glu288, desempenhando um papel fundamental na organização do complexo catalítico durante a ligação do ADP ou ATP.
Conclusão final e resumida do funcionamento do Domínio Biotina carboxilase (BC)
A biotina carboxilase (BC) constitui o ponto de partida catalítico da acetil-CoA carboxilase e representa o elemento que é responsável pela ativação química do CO₂ no contexto da lipogênese. A sua organização estrutural altamente conservada, baseada na cooperação funcional entre os domínios A, B e C, é que estabelece um sítio catalítico capaz de coordenar ATP, bicarbonato, biotina e íon magnésio de uma forma precisa e ordenada. A formação do intermediário carboxifosfato, sua decomposição controlada e a geração do CO₂ reativo é depende diretamente dessa arquitetura tridimensional e da dinâmica conformacional do domínio B, que regula o fechamento transitório do sítio ativo e também assegura a eficiência da reação.
E bom deixar claro que a BC não atua de maneira isolada, mas é integrada ao domínio carreador de biotina (BCCP), ao qual a carboxil-biotina recém-formada é funcionalmente acoplada. A carboxilação da biotina não representa o término da reação, mas é a geração de um intermediário químico móvel que conecta a ativação do CO₂ à etapa subsequente catalisada pela carboxiltransferase (CT). Nesse sentido, a BC estabelece qual será a direção e a viabilidade de todo o ciclo catalítico da acetil-CoA carboxilase, determinando se o fluxo de carbono será efetivamente canalizado para a síntese de malonil-CoA.
Além disso, a natureza dimérica da BC e o mecanismo catalítico que é do tipo flip-flop reforçam que a eficiência enzimática depende não apenas da integridade do sítio ativo individual, mas também de uma coordenação estrutural entre os monômeros. Essa organização tem a fução de assegurar alternância catalítica, estabilidade estrutural e a continuidade do ciclo reacional. Portanto, a biotina carboxilase deve ser compreendida como o núcleo iniciador e também organizador da atividade da acetil-CoA carboxilase, cuja a função transcende a uma simples carboxilação da biotina, estabelecendo a base mecanística indispensável para a lipogênese celular e, no contexto tumoral, para a reprogramação metabólica associada ao câncer de mama.
Biotina carboxilase (BCCP)
Sub-processo 2 – Transporte funcional da biotina entre os sítios catalíticos da ACC
A proteína carreadora de carboxil-biotina (BCCP) é o componente catalítico da acetil-CoA carboxilase (ACC) que tem a função de transportar a biotina até o sítio ativo da biotina carboxilase (BC), onde vai ocorrer sua carboxilação. Em seguida, a carboxil-biotina formada é translocada para o sítio ativo da carboxiltransferase (CT), e é lá no qual, onde vai ocorrer a transferência do grupo carboxil da biotina para o acetil-CoA, dando origem a molécula de malonil-CoA.
FUNÇÃO – Transporte e entrega da biotina carboxilada entre BC e CT
Entrada: biotina ligada covalentemente ao domínio BCCP
Por que passa por este processo: a reação catalítica da ACC ocorre em dois sítios distintos (BC e CT), exigindo um carreador móvel
Produto final: posicionamento eficiente da biotina carboxilada no sítio ativo da CT
Funcionamento da (BCCP) é dividido em 11 partes:
Parte -1 (Organização estrutural do domínio biotinil do BCCP)
A BCCP é constituída por 156 resíduos de aminoácidos (~16,7 kDa) e tem um domínio C-terminal que é também altamente conservado, denominado domínio biotinoil, que são presente em proteínas que são dependentes de biotina. Esse domínio é responsável pela ligação covalente da biotina e que também desempenha papel essencial para o transporte do grupo carboxil entre os sítios catalíticos da acetil-CoA carboxilase. Apesar das variações de tamanho e sequência entre espécies, a sua organização estrutural e a função desse domínio são amplamente conservadas.
FUNÇÃO – Ancoragem covalente e transporte do cofator biotina
Entrada: domínio BCCP não biotinilado
Por que passa por este processo: a biotina precisa estar covalentemente ligada para atuar como carreador funcional
Produto final: domínio BCCP biotinilado e estruturalmente funcional
Parte -2 (Homologia estrutural com domínios lipoil e função carreadora)
O domínio biotinil apresenta uma homologia estrutural com os domínios lipoil são encontrados em enzimas que utilizam o ácido lipóico como coenzima. Em ambos os casos, o cofator é ligado covalentemente a um resíduo específico de lisina que é por meio de uma ligação amida. Essa ligação vai permitir que a biotina e o ácido lipóico tem a função de atuar como carreadores de grupos químicos entre diferentes sítios catalíticos dessa mesma enzima ou entre subunidades que sejam de complexos multienzimáticos.
FUNÇÃO – Viabilização do transporte de grupos químicos entre sítios catalíticos
Entrada: domínio biotinil estruturalmente organizado
Por que passa por este processo: a transferência catalítica exige um cofator móvel covalentemente ligado
Produto final: capacidade funcional de transporte de grupos carboxila
Parte -3 (Especialização funcional das proteínas dependentes de biotina)
As proteínas que são dependentes de biotina tem o papel de exercer a atividade de carboxilases, catalisando reações de carboxilação dependentes de ATP. Em contraste, enzimas que utilizam o ácido lipóico também desempenham funções de lipoamida aciltransferase, com a função de participa da transferência de grupos acila. Esse tipo de mecanismo é utilizado nos complexos piruvato desidrogenase, 2-oxoglutarato desidrogenase e no complexo envolvido no metabolismo de aminoácidos de cadeia ramificada (BCKDK).
FUNÇÃO – Execução de reações de carboxilação dependentes de ATP
Entrada: cofator biotina funcionalmente ligado
Por que passa por este processo: a função catalítica das carboxilases depende da ativação e transporte do CO₂
Produto final: reações de carboxilação metabolicamente ativas
Parte – 4 (Biotinilação covalente no motivo estrutural conservado)
O sítio de biotinilação das proteínas carboxilases dependentes de biotina corresponde a uma sequência estrutural altamente conservada, composta pelos resíduos (Ala/Val)–Met–Lys–(Met/Leu). Esse motivo define o local específico no qual ocorre a ligação covalente da biotina ao domínio carreador de biotina da enzima, por meio do grupo ε-amino do resíduo de lisina central. A ligação formada é do tipo amida e é essencial para permitir a atividade catalítica da enzima, uma vez que a biotina atua como um cofator que é responsável pelo transporte do grupo carboxila entre sítios catalíticos distintos.
FUNÇÃO – Fixação covalente da biotina no domínio carreador
Entrada: sequência consenso (Ala/Val)–Met–Lys–(Met/Leu)
Por que passa por este processo: a biotina só é funcional quando ligada covalentemente
Produto final: biotina ancorada por ligação amida funcional
Parte – 5 (Função dinâmica do BCCP como braço móvel catalítico)
O domínio carreador de biotina (BCCP) é uma subunidade estruturalmente especializada cuja sua principal função é posicionar a biotina de forma adequada para a sequência de reações catalisadas pelas carboxilases. Após a ligação covalente da biotina à lisina específica, o cofator passa agora a atuar como um grupo funcional móvel, permitindo a transferência eficiente do CO₂ ativado entre o domínio biotina carboxilase e o domínio carboxiltransferase da enzima. Dessa forma, a biotinilação não é apenas uma modificação pós-traducional, mas sim um requisito estrutural que ´e indispensável para a atividade enzimática.
FUNÇÃO – Transferência física do CO₂ ativado entre BC e CT
Entrada: biotina covalentemente ligada ao BCCP
Por que passa por este processo: os sítios catalíticos são espacialmente separados
Produto final: entrega eficiente do grupo carboxila à CT
Parte – 6 (Organização estrutural β-sanduíche do domínio BCCP)
Estruturalmente, o domínio BCCP apresenta uma organização característica do tipo β-sanduíche, formada por cadeias β antiparalelas que conferem estabilidade ao núcleo estrutural da proteína. Esse arranjo estrutural é estabilizado por um conjunto de resíduos hidrofóbicos altamente conservados, que formam o núcleo interno do domínio. A conservação desse núcleo hidrofóbico é um elemento crítico para acontecer a manutenção da conformação tridimensional necessária ao correto posicionamento da biotina e à integridade funcional da enzima.
FUNÇÃO – Estabilidade conformacional do domínio carreador
Entrada: cadeias β antiparalelas conservadas
Por que passa por este processo: a estabilidade estrutural é essencial para a mobilidade funcional
Produto final: domínio BCCP estruturalmente íntegro
Parte – 7 (Exposição controlada do sítio de biotinilação)
O sítio de biotinilação localiza-se em uma região estrutural definida, associada a uma dobra do tipo β-hairpin, que expõe o resíduo de lisina para a reação de ligação covalente com a biotina. Essa conformação vai permitir o acesso do cofator ao grupo amino reativo, e ao mesmo tempo assegurará a estabilidade da ligação formada. A organização local dessa região é fundamental para garantir que a biotina permaneça firmemente ancorada, mas com flexibilidade suficiente para participar das reações catalíticas subsequentes.
FUNÇÃO – Acesso químico e estabilidade da ligação covalente
Entrada: dobra estrutural do tipo β-hairpin
Por que passa por este processo: a lisina precisa estar acessível e estabilizada
Produto final: biotina firmemente ancorada e funcional
Parte – 8 (Mobilidade conformacional do domínio BCCP)
Além do núcleo estrutural, o domínio BCCP também contem regiões flexíveis que desempenham papel funcional importante. Essas regiões conferem mobilidade conformacional ao domínio, permitindo que a biotina se desloque fisicamente entre os diferentes centros catalíticos da enzima durante o ciclo reacional. Essa mobilidade é um aspecto essencial do mecanismo catalítico das carboxilases dependentes de biotina e está diretamente relacionada à eficiência da carboxilação.
FUNÇÃO – Permitir o deslocamento físico da biotina durante o ciclo catalítico
Entrada: regiões estruturais flexíveis do BCCP
Por que passa por este processo: a catálise exige movimento entre sítios ativos
Produto final: eficiência catalítica global aumentada
Parte – 9 (Papel estrutural da biotinilação na estabilidade do BCCP)
A ausência de biotinilação compromete a estabilidade estrutural do domínio BCCP e reduz significativamente a atividade catalítica da enzima. A função da biotina ligada é contribui para a organização conformacional do domínio, favorecendo um estado estrutural funcionalmente ativo. Dessa forma, a biotinilação assegura não apenas a presença do cofator, mas também a manutenção da arquitetura estrutural necessária ao funcionamento adequado da enzima.
FUNÇÃO – Manutenção da conformação cataliticamente ativa
Entrada: domínio BCCP biotinilado
Por que passa por este processo: a ausência do cofator compromete a estrutura
Produto final: domínio funcionalmente estável
Parte – 10 (Integração estrutural e funcional BC–BCCP)
A interação entre o domínio biotina carboxilase (BC) e o domínio carreador de biotina (BCCP) é um elemento central para o funcionamento das carboxilases dependentes de biotina. Essa interação assegura o que aconteça o acoplamento físico entre o sítio de ativação do CO₂ e o domínio responsável pelo transporte da biotina, permitindo a coordenação eficiente das etapas catalíticas da enzima. A afinidade elevada da biotina por proteínas de ligação específicas evidencia a estabilidade da associação do cofator ao domínio BCCP e reforça a importância estrutural dessa interação para a organização do complexo enzimático.
FUNÇÃO – Acoplamento entre ativação do CO₂ e transporte do cofator
Entrada: domínios BC e BCCP estruturalmente íntegros
Por que passa por este processo: a reação depende de coordenação interdomínios
Produto final: ciclo catalítico funcional das carboxilases
Parte – 11 (Integração estrutural e funcional entre BC e BCCP no controle catalítico das carboxilases dependentes de biotina)
Visão geral do papel estrutural do domínio BCCP nas carboxilases dependentes de biotina
Em conjunto, a estrutura do domínio BCCP e o processo de biotinilação constituem elementos centrais para o funcionamento das carboxilases dependentes de biotina. A integridade desse sistema estrutural é determinante para a atividade enzimática e para o controle das vias metabólicas nas quais essas enzimas estão envolvidas, incluindo aquelas relacionadas à síntese de ácidos graxos.
- Interação funcional entre os domínios BC e BCCP
A interação entre o domínio biotina carboxilase (BC) e o domínio carreador de biotina (BCCP) é um elemento central do funcionamento das carboxilases dependentes de biotina. Porque Essa interação é que assegura o acoplamento físico entre o sítio de ativação do CO₂ e o domínio responsável pelo transporte da biotina, permitindo uma coordenação eficiente das etapas catalíticas da enzima. A afinidade elevada da biotina por proteínas de ligação específicas evidencia a estabilidade da associação do cofator ao domínio BCCP e reforça a importância estrutural dessa interação para a organização do complexo enzimático.
- Organização estequiométrica e dinâmica conformacional do complexo BC–BCCP
O complexo funcional formado entre BC e BCCP apresenta uma organização estequiométrica definida, na qual múltiplas moléculas de BCCP se associam ao domínio BC, refletindo a necessidade de mobilidade do cofator biotina durante o ciclo catalítico. Essa organização favorece a alternância do domínio BCCP entre diferentes estados conformacionais, permitindo que a biotina seja posicionada repetidamente no sítio ativo do domínio BC para a reação de carboxilação dependente de ATP.
- Contribuição estrutural da região N-terminal do domínio BCCP
A região N-terminal do domínio BCCP desempenha papel estrutural relevante na interação com o domínio BC. Essa porção da proteína contribui para o reconhecimento intermolecular e para o posicionamento adequado do domínio carreador em relação ao sítio catalítico do BC. Alterações estruturais nessa região comprometem a formação do complexo funcional, evidenciando sua importância para a eficiência catalítica da enzima como um todo.
- Interface molecular e caráter dinâmico da interação BC–BCCP
Do ponto de vista estrutural, a interação entre BC e BCCP envolve contatos específicos entre resíduos localizados na superfície de ambos os domínios. Esses contatos incluem interações polares e hidrofílicas que estabilizam o complexo transitório formado durante o ciclo catalítico. A interface de interação é suficientemente estável para permitir a associação funcional, mas mantém caráter dinâmico, compatível com a necessidade de dissociação e reassociação do domínio BCCP ao longo do processo catalítico.
- Papel do domínio C-terminal do BCCP e alinhamento da biotina
O domínio C-terminal do BCCP, que abriga o sítio de biotinilação, também participa da interação com o domínio BC. Essa região contribui para o alinhamento estrutural do cofator biotina em relação ao sítio ativo do BC, assegurando que a transferência do grupo carboxila ocorra de forma eficiente. A organização tridimensional desse domínio favorece a exposição controlada da biotina, mantendo-a acessível para a reação catalítica sem comprometer a estabilidade estrutural da proteína.
- Arquitetura estrutural do domínio BCCP em enzimas eucarióticas
Em enzimas eucarióticas, o domínio BCCP apresenta arquitetura estrutural globalmente semelhante à observada em outros sistemas de carboxilases dependentes de biotina, preservando o arranjo em folhas β e o núcleo hidrofóbico característico do subdomínio biotinil. No entanto, diferenças estruturais específicas refletem adaptações funcionais próprias do contexto celular eucariótico, sem alterar o princípio fundamental de funcionamento do domínio carreador de biotina.
- Biotinilação, flexibilidade conformacional e função carreadora da biotina
No domínio BCCP eucariótico, a biotina encontra-se ligada covalentemente a um resíduo específico de lisina, posicionada de modo a não estabelecer interações rígidas com resíduos adjacentes da proteína. Essa característica confere maior flexibilidade conformacional ao cofator, permitindo que ele atue como um elemento móvel essencial para a transferência do grupo carboxila entre os domínios catalíticos da enzima. A ausência de interações estruturais restritivas entre a biotina e a proteína reforça a natureza dinâmica do domínio BCCP.
- Integração estrutural e base mecanística das carboxilases dependentes de biotina
Em conjunto, a organização estrutural dos domínios BC e BCCP e a interação funcional entre eles constituem a base mecanística das carboxilases dependentes de biotina. A integridade dessa interação é indispensável para a atividade catalítica da enzima e para o controle eficiente das vias metabólicas nas quais essas carboxilases estão envolvidas, incluindo aquelas associadas à síntese de ácidos graxos.
Conclusão final e resumida do funcionamento do Domínio carreador de biotina (BCCP)
Em síntese, o domínio carreador de biotina (BCCP) constitui um elemento estrutural e funcional indispensável para a atividade das carboxilases dependentes de biotina. Pois a sua arquitetura tridimensional, associada à biotinilação covalente em um resíduo específico de lisina, confere ao cofator biotina a flexibilidade conformacional que é necessária para atuar como elemento móvel ao longo do ciclo catalítico. A interação dinâmica e altamente coordenada entre o BCCP e o domínio biotina carboxilase (BC) assegura o acoplamento eficiente entre a ativação do CO₂ e a transferência do grupo carboxila, estabelecendo a base mecanística que sustenta a eficiência catalítica e o controle funcional dessas enzimas nas vias metabólicas associadas, incluindo a síntese de ácidos graxos.
Carboxiltransferase (CT)
Sub-processo 3 – Definição do arcabouço catalítico da CT
O domínio carboxiltransferase (CT) é o componente da acetil-CoA carboxilase que é responsável pela transferência do grupo carboxila da biotina para o acetil-CoA, resultando na formação da molecula de malonil-CoA. Estruturalmente, esse domínio pertence à superfamília das crotonases, cujos membros compartilham uma arquitetura conservada baseada em repetições do motivo ββα. Nesse arranjo estrutural, duas cadeias β aproximadamente perpendiculares entre si são circundadas por hélices α, formando um arcabouço estável e funcionalmente versátil.
Entrada: domínio CT com arquitetura ββα
Por que passa por este processo: a transferência do grupo carboxila exige um arranjo estrutural conservado
Produto final: base estrutural apta à formação do sítio ativo
Funcionamento da (CT) é dividido em 07 partes:
Parte – 1 (Formação da cavidade catalítica central)
A organização estrutural do domínio CT é multimérica e composta por dois subdomínios estruturalmente relacionados, equivalentes aos domínios N-terminal e C-terminal presentes em enzimas de cadeia única. Esses subdomínios associam-se formando um arranjo tetramérico organizado como um dímero de dímeros, cuja sua estrutura global apresenta geometria semelhante a de uma pirâmide truncada. Essa conformação define uma cavidade central que se alarga progressivamente em direção à superfície da enzima, constituindo o ambiente estrutural necessário para o acesso e posicionamento dos substratos.
Entrada: subdomínios N-terminal e C-terminal associados
Por que passa por este processo: o posicionamento correto dos substratos requer um espaçocatalítico definido
Produto final: cavidade central funcional para ligação dos substratos
Parte – 2 (Estabilização estrutural e controle de acesso ao sítio ativo)
Cada subdomínio do CT é constituído por regiões helicoidais e folhas β que formam subdomínios funcionais distintos. Entre esses, destacam-se os subdomínios helicoidais, que são responsáveis pela estabilização do complexo, e uma região estrutural especializada que coordena um íon metálico por meio de um motivo do tipo dedo-de-zinco, que é formado por quatro resíduos de cisteína. Esse motivo não participa diretamente da ligação dos substratos, mas ele desempenha um papel estrutural que é essencial na organização do sítio ativo e no controle do acesso dos substratos à cavidade catalítica.
Entrada: regiões helicoidais, folhas β e motivo dedo-de-zinco
Por que passa por este processo: a catálise exige estabilidade conformacional e controle espacial
Produto final: sítio ativo estruturalmente organizado e regulado
Parte – 3 (Ajuste conformacional para ativação catalítica)
A atividade catalítica do domínio CT depende da formação de interfaces específicas entre os subdomínios. Essas interfaces apresentam diferentes graus de estabilidade, permitindo rearranjos conformacionais controlados durante o ciclo catalítico. Mais uma dessas interfaces é estruturalmente mais robusta e resulta do reposicionamento de subdomínios helicoidais, promovendo o empacotamento de hélices α e folhas β em uma região compacta que é conhecida como feixe de seis hélices. Esse feixe é estabilizado por resíduos hidrofóbicos conservados, que asseguram a conformação adequada para a catálise.
Entrada: interfaces entre subdomínios com diferentes estabilidades
Por que passa por este processo: a transferência do grupo carboxila requer rearranjos controlados
Produto final: feixe de seis hélices estabilizado para a catálise
Parte – 4 (Execução química da transferência do grupo carboxila)
Associada a essa região encontra-se uma plataforma catalítica formada por cadeias β provenientes de ambos os subdomínios. Essa plataforma abriga resíduos altamente conservados e envolvidos diretamente nas etapas químicas da reação, incluindo a estabilização de intermediários reativos e a liberação do produto final. A organização precisa dessas estruturas é determinante para a eficiência da transferência do grupo carboxila.
Entrada: resíduos catalíticos conservados organizados na plataforma β
Por que passa por este processo: a reação química depende do alinhamento preciso dos resíduos
Produto final: ambiente catalítico competente para a reação
Parte – 5 (Reconhecimento e posicionamento do acetil-CoA)
O sítio ativo do domínio CT fica em uma região profunda, que é descrita como um “cânion” estrutural, formado na interface entre os subdomínios. Nesse local ocorre o reconhecimento e a ligação do acetil-CoA. A base adenina do substrato interage com resíduos específicos de um dos subdomínios, enquanto que o grupo tiol da coenzima A é acomodado pelo subdomínio complementar. As paredes desse cânion são formadas por hélices α, enquanto o fundo é delimitado por cadeias β do motivo ββα, isto cria um ambiente adequado para uma reação catalítica.
Entrada: acetil-CoA
Por que passa por este processo: a orientação correta do substrato é essencial para a reação
Produto final: acetil-CoA ligado e posicionado no sítio ativo
Parte – 6 (Transferência e estabilização do grupo carboxila)
Durante essa reação, o grupo carboxila previamente ligado à biotina é transferido para o acetil-CoA. Esse processo envolve a desprotonação do grupo amida do acetil-CoA, levando à formação de um intermediário enolato que é altamente reativo. Resíduos específicos de glicina, posicionados estrategicamente no sítio ativo, participam da formação de canais oxiânion, que estabilizam tanto o intermediário imidato da biotina quanto o intermediário enolato do acetil-CoA. Essa estabilização é essencial para poder permitir a formação eficiente da molecula do malonil-CoA.
Entrada: carboxil-biotina e acetil-CoA ativado
Por que passa por este processo: intermediários instáveis precisam ser estabilizados para a reação prosseguir
Produto final: malonil-CoA formado
Parte – 7 (Conclusão do ciclo catalítico da ACC)
Em conjunto, o domínio carboxiltransferase apresenta uma organização estrutural altamente especializada, na qual a disposição precisa de subdomínios, interfaces e resíduos catalíticos garante que aja a transferência eficiente do grupo carboxila. A integridade estrutural do CT é portanto, fundamental para a atividade global da acetil-CoA carboxilase e para o controle das vias metabólicas que são associadas à síntese de ácidos graxos.
Entrada: malonil-CoA recém-formado
Por que passa por este processo: o produto deve ser liberado para continuidade metabólica
Produto final: integração da CT ao fluxo biossintético de ácidos graxos
Conclusão final e resumida do funcionamento do Domínio carboxiltransferase (CT)
O domínio carboxiltransferase (CT) constitui a etapa final e decisiva do ciclo catalítico da acetil-CoA carboxilase, sendo responsável pela transferência do grupo carboxila da carboxil-biotina para o acetil-CoA, originado na formação na molecula de malonil-CoA. Essa reação representa o ponto de conversão entre a ativação química do CO₂ e a sua incorporação efetiva ao metabolismo lipogênico, conferindo ao CT um papel central na determinação do fluxo biossintético de ácidos graxos.
Estruturalmente, o CT apresenta uma organização altamente conservada, típica da superfamília das crotonases, baseada em repetições do motivo ββα que formam um arcabouço catalítico estável e funcionalmente especializado. A disposição precisa dos subdomínios, aliada à orientação estratégica dos resíduos catalíticos no sítio ativo, que assegura o reconhecimento eficiente da carboxil-biotina e do acetil-CoA, bem como o alinhamento adequado dos grupos reativos para a transferência do grupo carboxila.
E importante indicar, que a atividade do CT depende diretamente da entrega correta e temporizada da carboxil-biotina pelo domínio BCCP, evidenciando que sua função não é isolada, mas integrada a um sistema catalítico coordenado. Caso haja alterações estruturais, desalinhamento de interfaces ou perturbações na dinâmica entre CT e BCCP comprometem a eficiência da reação, reduzindo a formação de malonil-CoA, isso vai impactar de forma direta a lipogênese celular.
Além de sua função catalítica, o domínio CT também atua como um ponto de controle funcional da acetil-CoA carboxilase, uma vez que sua eficiência determina a taxa final de produção de malonil-CoA e, consequentemente, a eficiencia do suprimento de precursores para a síntese de ácidos graxos. No contexto tumoral, especialmente no câncer de mama, essa etapa assume relevância ampliada, pois ela sustenta a demanda lipogênica elevada que é uma característica da reprogramação metabólica das células malignas.
Assim, o domínio carboxiltransferase representa o fechamento mecanístico do ciclo catalítico da acetil-CoA carboxilase, traduzindo a ativação do CO₂ em produto metabólico funcional. A sua integridade estrutural e a sua coordenação dinâmica com BC e BCCP são indispensáveis para o funcionamento pleno da enzima e também para o controle das vias lipogênicas associadas à progressão tumoral.
referências:
Acetil-CoA carboxilase
https://pt.wikipedia.org/wiki/Acetil-CoA_carboxilase
Thiago Estefano Rodrigues (regulação da Acetil-CoA carboxilase)
Acetil-CoA Carboxilases e Doenças
https://pmc.ncbi.nlm.nih.gov/articles/PMC8963101
Acetilcoenzima A
https://pt.wikipedia.org/wiki/Acetilcoenzima_A
Reprogramação do metabolismo de ácidos graxos no câncer de mama: uma revisão narrativa.
https://tbcr.amegroups.org/article/view/48710/html
Direcionando a captação e o metabolismo de ácidos graxos em células cancerígenas: uma estratégia promissora para o tratamento do câncer.
https://www.sciencedirect.com/science/article/pii/S0753332223013896
reprogramação do metabolismo de ácidos graxos no câncer
https://www.nature.com/articles/s41416-019-0650-z
A inibição da malonil-CoA descarboxilase é seletivamente citotóxica para células de câncer de mama humano.
https://pubmed.ncbi.nlm.nih.gov/19543323